- Классификация веществ
- Простые и сложные вещества
- Основные классы неорганических веществ
- Бинарные соединения
- Запомни!
- Оксиды
- Основные оксиды
- Пример
- Амфотерные оксиды
- Пример
- Кислотные оксиды
- Пример
- Гидроксиды
- Основания
- Пример
- Амфотерные гидроксиды
- Пример
- Кислоты
- Пример
- Пример
- Названия кислот и кислотных остатков
- Полезные ссылки
- Дополнительные материалы
- Виды простых и сложных веществ
- Простые и сложные вещества в химии
- Классификация простых веществ
- Классы и номенклатура неорганических веществ
- Строение и химические свойства
- Химические свойства металлов и неметаллов
- Химические свойства благородных газов
- Строение и основные химические свойства сложных веществ
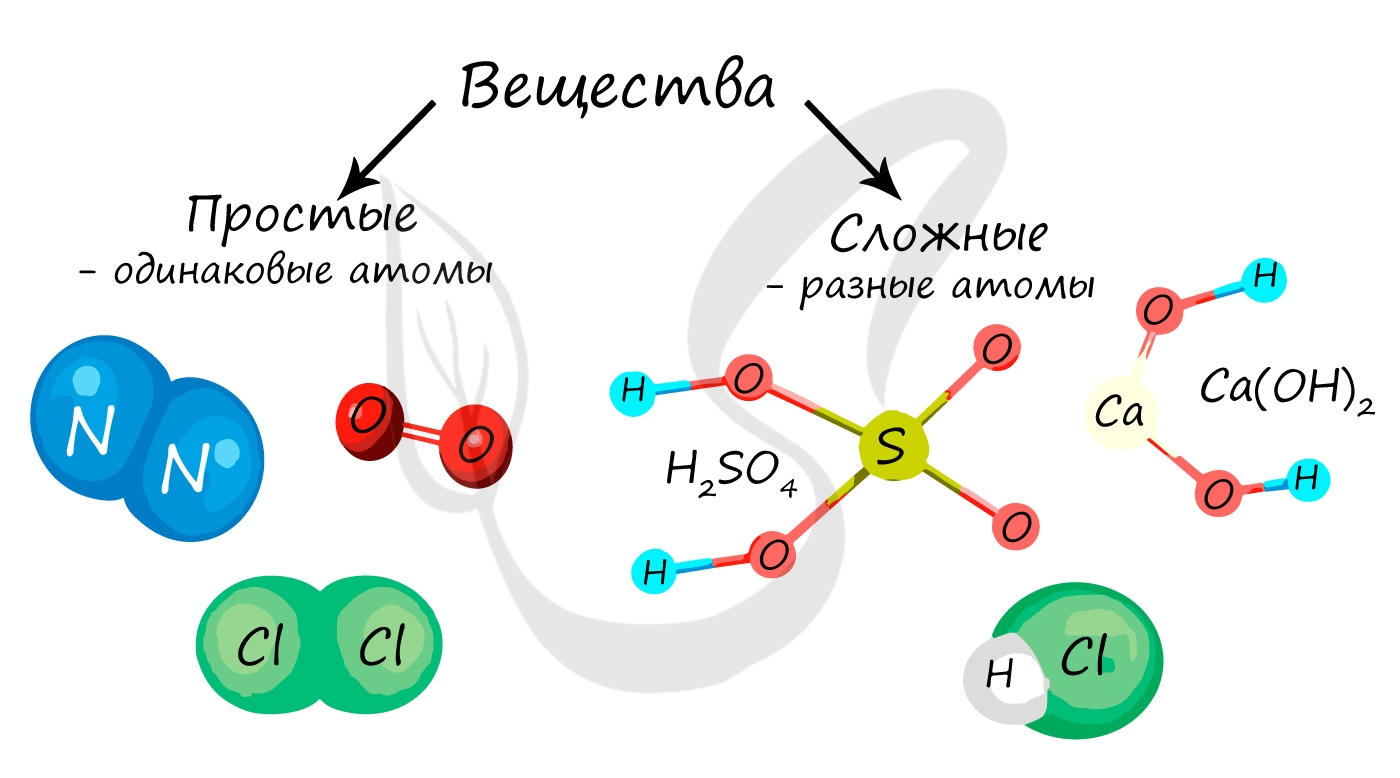
Классификация веществ
Вещество в химии — любая совокупность атомов и молекул. Вещества в химии подразделяются на простые и сложные.
Простые и сложные вещества
Простые вещества состоят из атомов одного химического элемента, то есть их образуют два и более одинаковых атома: H2, N2, O2, O3(озон), Mn, Fe.
Сложные вещества состоят из атомов двух и более видов: KMnO4, H2SO4, HCl.
Предмет химии (греч. chymos — сок)
У любой науки есть предмет изучения и методами, с помощью которых изучается предмет. Химия — наука о веществах, их превращениях и явлениях, которые сопровождают эти превращения.
Хочу заметить важную деталь: необходимо четко разделять химические и физические реакции. При химических реакциях происходят изменения в составе молекул: одни атомы сменяются другими, молекулы рвутся на части и собираются снова в обновленном виде.
При физических реакциях молекулы неизменны, связи атомов внутри них не подвергается изменениям.
К признакам химических реакций относится ряд критериев:
- Выделение газа
- Появление запаха
- Изменение окраски раствора или реагирующих веществ
- Выпадение осадка
- Образование воды
- Выделение тепла
- Поглощение тепла
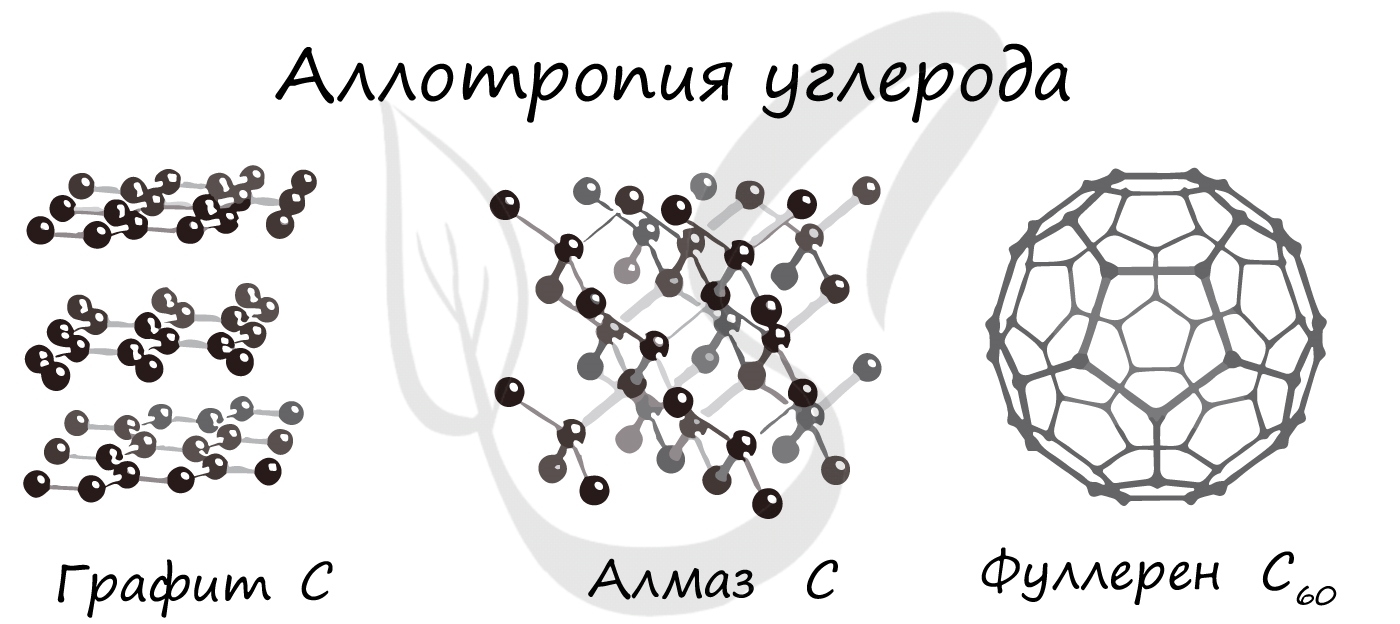
Аллотропия
Аллотропия (греч. allos — иной + tropos образ) — свойство некоторых химических элементов принимать различные физические формы, существовать в виде двух и более простых веществ.
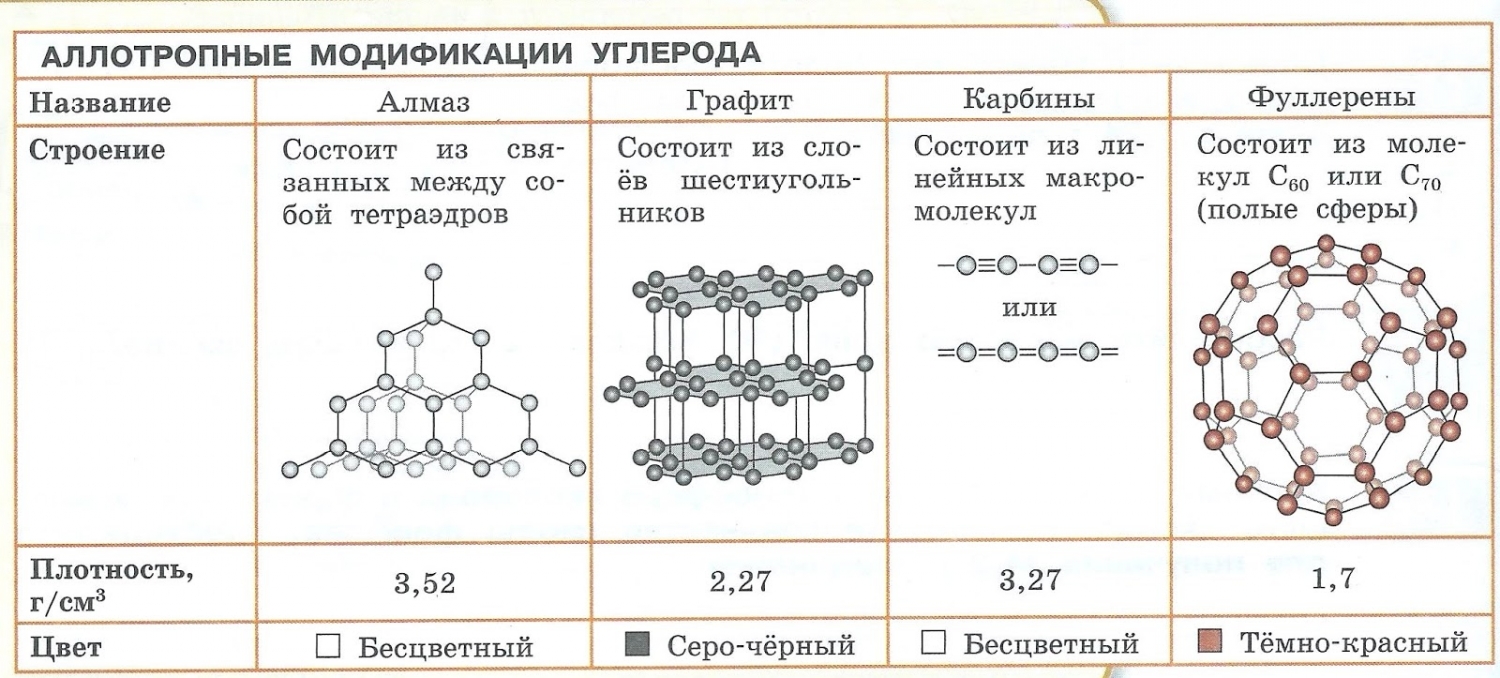
Такие уникальные способности имеются у углерода. Его известнейшие аллотропные модификации: алмаз, графит и фуллерен. В разделе химических связей мы вернемся к ним, однако будет хорошо, если вы уже сейчас запомните: алмаз и графит имеют атомное строение, фуллерен — молекулярное.
Обратите внимание: вы можете догадаться о строении веществ по их формуле. У фуллерена молекулу составляют 60 атомов углерода. Мы изучали, что молекула — это как минимум два атома, соединенных вместе. Таким образом, уже по формуле, очевидно, что строение фуллерена молекулярное.
Среди аллотропных модификаций фосфора выделяют: белый, красный и черный фосфор. Белый (P4) фосфор имеет молекулярное строение, а красный и черный (P∞) — атомное.
Аллотропные модификации серы включают ромбическую, моноклинную, и пластическую серу. Ромбическая (S8) и моноклинная сера (S8) имеют молекулярное строение. Пластическая сера (S∞) представляет собой длинные цепочки атомов, тем не менее также характеризуется молекулярным строением.
Надо заметить, что с течением времени, пластическая и моноклинная модификации серы, неустойчивые, превращаются в ромбическую, наиболее устойчивую.
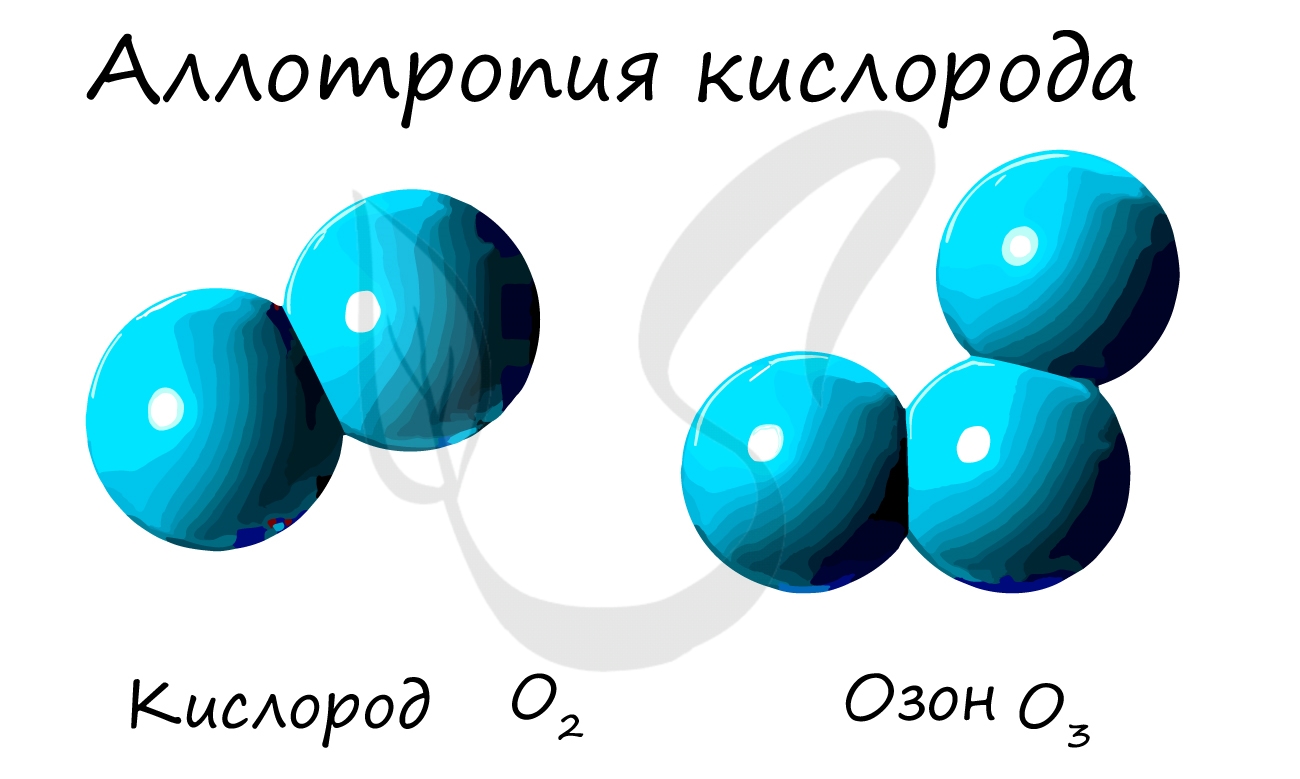
Из аллотропных модификаций кислорода наиболее известен озон (греч. ozo — иметь сильный запах). Озон — неустойчивая модификация кислорода, образуется в озоновом слое под действием ультрафиолетового излучения. Имеет молекулярное строение и формулу — O3.
Озон — ядовитый газ. Применяется как окислитель при отбеливании, при очистке воды и кондиционировании воздуха. В медицине существует целое направление, посвященное лечению с применение озона — озонотерапия.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Простые и сложные вещества
Простые вещества: молекулы состоят из атомов одного вида (атомов одного элемента).
Пример: H2, O2,Cl2, P4, Na, Cu, Au.
Сложные вещества (или химические соединения): молекулы состоят из атомов разного вида (атомов различных химических элементов).
Пример: H2O, NH3, OF2, H2SO4, MgCl2, K2SO4.
Аллотропия — способность одного химического элемента образовывать несколько простых веществ, различающихся по строению и свойствам.
- С — алмаз, графит, карбин, фуллерен.
- O — кислород, озон.
- S — ромбическая, моноклинная, пластическая.
- P — белый, красный, чёрный.
Явление аллотропии вызывается двумя причинами:
- Различным числом атомов в молекуле, например кислород O2 и озон O3.
- Образованием различных кристаллических форм, например алмаз, графит, карбин и фуллерен (смотри рисунок выше).
Основные классы неорганических веществ
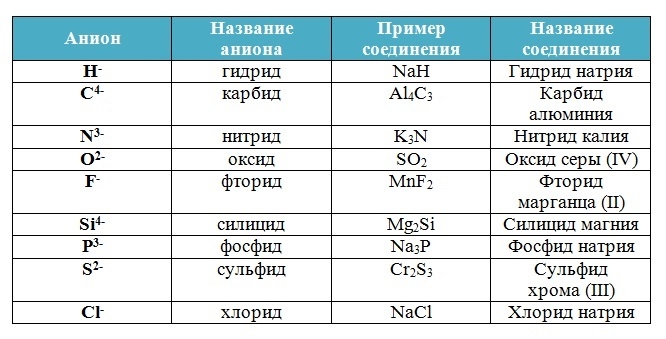
Бинарные соединения
Вещества, состоящие из двух химических элементов называются бинарными (от лат. би – два) или двухэлементными.
Названия бинарных соединений образуют из двух слов – названий входящих в их состав химических элементов.
Первое слово обозначает электроотрицательную часть соединения – неметалл, его латинское название с суффиксом –ид стоит всегда в именительном падеже.
Второе слово обозначает электроположительную часть – металл или менее электроотрицательный элемент, его название стоит в родительном падеже, затем указывается степень окисления (только в том случае, если она переменная):
Запомни!
Оксиды
Оксиды — сложные вещества, состоящие из двух химических элементов, один из которых кислород в степени окисления -2.
Общая формула оксидов: ЭхОу
Основные оксиды
Основные оксиды — оксиды, которым соответствуют основания.
Основные оксиды образованы металлом со степенью окисления +1, +2.
Пример
Соответствие основных оксидов и оснований
- Na2O — Na2(+1)O(-2) — NaOH
- MgO — Mg(+2)O(-2) — Mg(OH)2
- FeO — Fe(+2)O(-2) — Fe(OH)2
- MnO — Mn(+2)O(-2) — Mn(OH)2
Амфотерные оксиды
Амфотерные оксиды — оксиды, которые в зависимости от условий проявляют либо основные, либо кислотные свойства.
Амфотерные оксиды образованы металлом со степенью окисления +3, +4, а также некоторыми металлами (Zn, Be) со степенью окисления +2.
Пример
Кислотные оксиды
Кислотные оксиды — оксиды, которым соответствуют кислоты.
Кислотные оксиды образованы неметаллом, а также металлом со степенью окисления +5, +6, +7.
Пример
Соответствие кислотных оксидов и кислот
- SO3 — S(+6)O3(-2) — H2SO4
- N2O5 — N2(+5)O5(-2) — HNO3
- CrO3 — Cr(+6)O3(-2) — H2CrO4
- Mn2O7 — Mn2(+7)O7(-2) — HMnO4
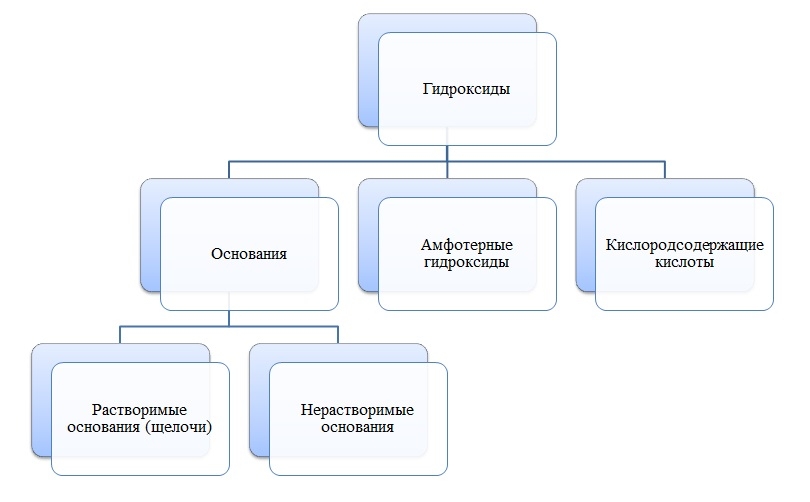
Гидроксиды
Гидроксиды — сложные вещества, состоящие из трех элементов, два из которых водород со степенью окисления +1 и кислород со степенью окисления -2.
Общая формула гидроксидов: ЭхОуНz
Основания
Основания — сложные вещества, состоящие из ионов металла и одной или нескольких гидроксо-групп (ОН-).
В основаниях металл имеет степень окисления +1, +2 или вместо металла стоит ион аммония NH4+
Пример
NaOH, NH4OH, Ca(OH)2
Амфотерные гидроксиды
Амфотерные гидроксиды — сложные вещества, которые в зависимости от условий проявляют свойства оснований или кислот.
Амфотерные гидроксиды имеют металл со степенью окисления +3, +4, а также некоторые металлы (Zn, Be) со степенью окисления +2.
Пример
Zn(OH)2, Be(OH)2, Al(OH)3, Cr(OH)3
Кислоты
Кислоты — сложные вещества, состоящие из атомов водорода и кислотных остатков.
В состав кислот входит неметалл или металл со степенью окисления +5, +6, +7.
Пример
H2SO4, HNO3, H2Cr2O7, HMnO4
Соли- соединения, состоящие из катионов металлов (или NH4+) и кислотных остатков.
Общая формула солей: MexAcy
- Me — металл
- Ac — кислотный остаток
Пример
KNO3 — нитрат калия
(NH4)2SO4 — сульфат аммония
Mg(NO3)2 — нитрат магния
Названия кислот и кислотных остатков
| Кислота | Кислотный остаток | ||
| Название | Формула | Название | Формула |
| Соляная (хлороводородная) | HCl | Хлорид | Cl(-) |
| Плавиковая (фтороводородная) | HF | Фторид | F(-) |
| Бромоводородная | HBr | Бромид | Br(-) |
| Иодоводородная | HI | Иодид | I(-) |
| Азотистая | HNO2 | Нитрит | NO2(-) |
| Азотная | HNO3 | Нитрат | NO3(-) |
| Сероводородная | H2S | Сульфид Гидросульфид | S(2-) HS(-) |
| Сернистая | H2SO3 | Сульфит Гидросульфит | SO3(2-) HSO3(-) |
| Серная | H2SO4 | Сульфат Гидросульфат | SO4(2-) HSO4(-) |
| Угольная | H2CO3 | Карбонат Гидрокарбонат | СО3(2-) НСО3(-) |
| Кремниевая | H2SiO3 | Силикат | SiO3(2-) |
| Ортофосфорная | H3PO4 | Ортофосфат Гидроортофосфат Дигидроортофосфат | РО4(3-) НРО4(2-) Н2РО4(-) |
| Муравьиная | НСООН | Формиат | НСОО(-) |
| Уксусная | СН3СООН | Ацетат | СН3СОО(-) |
Полезные ссылки
Дополнительные материалы
Станьте первым, кто оставит
комментарий к данному материалу.
Источник
Виды простых и сложных веществ
Простые и сложные вещества в химии
В неорганической химии вещества по составу делятся на простые и сложные.
- состоят из атомов одного химического элемента: сера S, углерод С, железо Fe, серебро Ag;
- подразделяют на металлы и неметаллы (включая благородные газы).
Сложные вещества — соединения:
- состоят из атомов двух или более химических элементов: Na2O, HCl, CuSO4;
- подразделяют на: оксиды, основания, кислоты и соли.
Классификация простых веществ
1. Простые вещества условно делят на две группы: металлы и неметаллы.
Неметаллы в Периодической системе — это все элементы VIII А-группы (благородные газы) и VII А-группы (галогены), элементы VI А-группы (кроме полония), элементы V А-группы: азот, фосфор, мышьяк; углерод, кремний (IV А-группа); бор (III А-группа), а также водород. Остальные элементы относят к металлам.
Отличия свойств металлов и неметаллов приведены в таблице 1:
| металлы | неметаллы | ||
| Тип химической связи | металлическая | ковалентная неполярная | |
| Кристаллическая решётка | металлическая | атомная или молекулярная | |
| Физические свойства | Агрегатное состояние | твёрдые, кроме жидкой ртути Hg |
|
| Блеск | металлический блеск | не обладают блеском (исключение: йод J2 и графит) | |
| Способность проводить тепло и электрический ток | хорошие проводники | плохо проводят тепло, не проводят ток — диэлектрики (исключение: графит, кремний Si и черный фосфор) | |
| Прочность, ковкость, пластичность | характерно для всех металлов (исключение: хром Cr, марганец Mn, сурьма Sb) | в твердом состоянии хрупкие | |
| Цвет | серебристо-белый, серебристо-серый (исключение: красная медь Cu, желтое золото Au и некоторые др.) | разный: почти черный йод J2, желтая сера S, черный, белый и красный фосфор P, бесцветные кислород O2, азот N2 | |
| Способность к аллотропии | слабая; некоторые металлы: железо Fe, олово Sn, лантаноиды и актиноиды. | хорошая; много модификаций у углерода С (графит, фуллерен, алмаз, карбин и др.); фосфора P (белый, чёрный, красный); серы S (кристаллическая, пластическая) | |
| Аллотропия — способность некоторых элементов существовать в виде двух или нескольких простых веществ (аллотропных модификаций), отличающихся по строению и свойствам. | |||
Амфотерные элементы находятся в А-группах Периодической системы: бериллий Be, алюминий Al, галлий Ga, германий Ge, олово Sn, свинец Pb, сурьма Sb, висмут Bi, полоний Po и др., а также большинство элементов Б-групп: хром Cr, марганец Mn, железо Fe, цинк Zn, кадмий Cd, золото Au и др., проявляют и металлические (оснóвные для соединений), и неметаллические (кислотные для соединений) свойства.
Благородные (инертные) газы (VIII А-группа Периодической системы): гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe и радиоактивный радон Rn:
- обнаруживаются в воздухе, в малых количествах — в воде, горных породах, природных газах;
- не имеют цвета, вкуса и запаха;
- крайне химически инертны;
- используются в источниках света для создания освещения различных цветов (Ne — огненно-красный, Xe— синевато-серый, тусклый, Ar — фиолетово-голубой и др).
2. Сложные соединения и их отличия от простых веществ.
Сложные вещества бывают органические, в основе которых лежит углерод, и неорганические (безуглеродные и некоторые углеродсодержащие соединения: карбиды, карбонаты, оксиды углерода и другие). Неорганические чаще всего подразделяют на оксиды, основания, кислоты и соли.
Главные отличия сложных неорганических веществ:
- Свойства элементов, входящих в соединение, не сохраняются. Например, металл кальций Ca и неметалл хлор Cl2. Каждому из этих простых веществ присущи свои характеристики. А соль CaCl2 имеет новые, отличные от характеристик простых веществ, свойства, сходные со свойствами класса солей.
- В ходе химических реакций сложное вещество может быть получено или разложено на составные части.
- Количественный состав сложного соединения всегда одинаков, независимо от места нахождения и способа получения (для веществ молекулярного состава).
Классификация неорганических соединений и их основные свойства приведены в таблице 2.
| Оксиды | Основания | Кислоты | Соли | |
| Составляющие | Элемент Э+кислород со степенью окисления -2 | Катион металла+гидроксид-анион OH- | атом водорода, способный замещаться на металл+кислотный остаток K | катион металла Me+анион кислотного остатка K |
| Формула | ЭnOm | Me+n(OH-)n | HnК | Me+nK-m |
| Примеры | Li2O, MgO, Fe2O3, CO2 | KOH, Ca(OH)2, Al(OH)3 | HCl, H2SO4, H3PO4 | NaNO3, CaCO3, Al2(SO4)3 |
| Агрегатное состояние |
| твёрдые: NaOH, Mg(OH)2 |
| твёрдые: KNO3, CaCO3, NaCl |
| По составу бывают: |
|
|
|
|
Классы и номенклатура неорганических веществ
Номенклатура — способ называния веществ.
Химическая формула — представление состава вещества с использованием символов химических элементов, числовых индексов и других знаков. Химическое название определяется составом вещества и изображается с помощью слова или группы слов. Названия строятся по номенклатурным правилам, с использованием русских названий элементов, кроме случаев, когда традиционно употребляются латинские корни (таблица 3):
| Ag — аргент | C — карб, карбон | H — гидр, гидроген | N — нитр | Pb — плюмб, | Si — сил, силик, силиц |
| As — арс, арсен | Cu — купр | Hg — меркур | Ni — никкол | S — сульф | Sn -станн |
| Au — аур | Fe — ферр | Mn — манган | O — окс, оксиген | Sb — стиб | |
| Например, оксид натрия Na2O, карбонат кальция CaCO3, перманганат калия KMnO4 | |||||
- Названия простых веществ чаще всего совпадают с русскими названиями соответствующих химических элементов. По необходимости к ним добавляется числовая греческая приставка: моно — 1, ди (латинский) — 2, три — 3, тетра — 4, пента — 5, гекса — 6, гепта — 7, окта — 8, нона (латинский) — 9, дека — 10. Например, (моно) кальций Ca, (моно) медь Cu, дикислород O2, трикислород O3, тетрафосфор P4. Исключение: аллотропные модификации: углерода С — графит, сажа, алмаз; кислорода — озон O3.
- Названия сложных веществ составляют по химической формуле справа налево. Для каждого класса веществ существуют свои правила составления формул и названий:
- формула оксидов: ЭnOm, где n и m — числовые индексы, определяющиеся степенями окисления элементов. Например,
Li+1 и O-2→ Li2O; Al+3 и O-2→ Al2O3; N+5 и O-2→ N2O5.
Название оксида: слово «оксид» в именительном падеже + название элемента Э в родительном падеже: оксид лития Li2O, оксид алюминия Al2O3.
Если элемент образует несколько оксидов, то в конце добавляют степень окисления римскими цифрами, заключая их в скобки:
- P2O5 — пентаоксид (ди)фосфора или оксид фосфора (V), читается: «оксид фосфора пять»;
- Fe2O3 — триоксид (ди)железа или оксид железа (III), читается: «оксид железа три».
Оксиды, которым соответствуют кислоты, также называют ангидридами: серный ангидрид SO3, азотный ангидрид N2O5 и др.
- формула оснований: Me+n(OH-)n, где нижний индекс n — количество гидроксид-анионов OH-.
K+1 и OH- → KOH, Mg+2 и OH- → Mg(OH)2.
Название: слово «гидроксид» в именительном падеже + название элемента в родительном падеже: гидроксид калия, гидроксид магния.
Если элемент образует несколько гидроксидов, то в конце добавляют степень окисления римскими цифрами, заключая их в скобки:
Fe(OH)2 — гидроксид железа (II), Cr(OH)3 — гидроксид хрома (III).
- формула кислот HnК, где K — кислотный остаток.
Названия бескислородных кислот: корень русского названия элемента, образующего кислоту + суффикс «о» + «-водородная кислота», например: HBr — бромоводородная кислота, HCl — хлороводородная кислота, H2S — сероводородная кислота.
Названия кислородсодержащих кислот: русское название образующего элемента + «кислота», с учетом правил:
- Если элемент находится в высшей степени окисления, то окончание будет «-ная» или «-овая»: H2SO4 — серная кислота, H3AsO4 — мышьяковая кислота. Окончание меняется с понижением степени окисления в последовательности: «-оватая» (HClO3— хлорноватая кислота), «-истая» (HClO2— хлористая кислота), «-оватистая» (HClO— хлорноватистая кислота).
- Если оксиду соответствует не одна кислота, то к названию кислоты с минимальным числом атомов кислорода, добавляется приставка «мета», а к названию кислоты с максимальным числом атомов кислорода — «орто», например, HPO3 — метафосфорная кислота, H3PO4 — ортофосфорная кислота.
Названия наиболее распространенных кислот и их остатков приведены в таблице 4:
| Формула и название кислоты | Название кислотного остатка, образующего соль |
| HAlO2 метаалюминиевая | метаалюминат |
| H3AlO3 ортоалюминиевая | ортоалюминат |
| HAsO3 метамышьяковая | метаарсенат |
| H3AsO4 ортомышьяковая | ортоарсенат |
| H3BO3 ортоборная | ортоборат |
| HBr бромоводородная | бромид |
| HBrO бромноватистая | гипобромит |
| HBrO3 бромноватая | бромат |
| HCN циановодородная | цианид |
| H2CO3 угольная | карбонат |
| HCl хлороводородная | хлорид |
| HClO хлорноватистая | гипохлорит |
| HClO2 хлористая | хлорит |
| HClO3 хлорноватая | хлорат |
| HClO4 хлорная | перхлорат |
| HF фтороводородная | фторид |
| HJ йодоводородная | йодид |
| HMnO4 марганцовая | перманганат |
| HNO2 азотистая | нитрит |
| HNO3 азотная | нитрат |
| HPO3 метафосфорная | метафосфат |
| H3PO4 ортофосфорная | ортофосфат |
| H2S сероводородная | сульфид |
| H2SO3 сернистая | сульфит |
| H2SO4 серная | сульфат |
| H2SiO3 метакремниевая | метасиликат |
| H3SiO4 ортокремниевая | ортосиликат |
- формула солей: MemKn
Название образуется в зависимости от типа соли.
- Средние соли — наименование кислотного остатка в именительном падеже + наименование катиона в родительном падеже, если необходимо, добавляется степень окисления: хлорид натрия NaCl, сульфат меди (II) CuSO4 и т.д.
- Кислые (только для многоосновных кислот) — приставка «гидро», при необходимости добавляется числовое значение (ди—, три—, тетра— и т.д.) + название кислотного остатка + название катиона: гидрокарбонат натрия NaHCO3, дигидроортофосфат бария Ba(H2PO4)2.
- Оснóвные — приставка «гидроксо» с числовым значением, если необходимо + название кислотного остатка + название катиона: гидроксохлорид магния MgOHCl, дигидроксохлорид железа (III) Fe(OH)2Cl.
- Двойные — анион в именительном падеже + катионы через дефис в родительном падеже: ортофосфат аммония—магния NH4MgPO4; метасиликат алюминия—лития LiAl(SiO3)2.
- Смешанные — название анионов через дефис в именительном падеже + название катиона в родительном падеже: хлорид-гипохлорит кальция Ca(ClO)Cl; нитрат-йодат натрия Na2IO3(NO3).
- Комплексные — название катиона в именительном падеже + название аниона в родительном падеже: хлорид диамминсеребра (I) [Ag(NH3)2]Cl; тетрагидроксоалюминат натрия Na[Al(OH)4].
- номенклатура бинарных соединений.
Бинарные соединения — сложные вещества, состоящие из двух элементов. В таких соединениях встречается два типа химической связи: ковалентная полярная (для неметаллов и некоторых амфотерных элементов) или ионная (для солей бескислородных кислот).
Названия строятся по схеме: к корню более электроотрицательного элемента добавляется окончание -ид (оксид, гидрид, карбид и т.д.) в именительном падеже + название второго элемента в родительном падеже, при необходимости добавляется числовое значение степени окисления: CS2 — дисульфид углерода или сульфид углерода (IV), MnF4 — тетрафторид марганца или фторид марганца (IV).
Для некоторых есть тривиальные названия: NH3 — аммиак, SiН4 — силан, PH3 — фосфин и др.
Строение и химические свойства
Простые вещества состоят из атомов одного химического элемента:
- одноатомные: благородные газы — гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe и радон Rn;
- двухатомные: водород H2, кислород O2, азот N2 и галогены: хлор Cl2, йод J2, бром Br2;
- трех и более атомные: озон O3, белый фосфор P4, кристаллическая (ромбическая и моноклинная) сера S8.
Порядок соединения атомов при образовании из них веществ обусловливает особенности строения веществ. Различают вещества молекулярного и немолекулярного строения. Немолекулярное строение имеют все металлы и большинство их соединений, графит, красный фосфор, алмаз, кремний Si и др. Большинство неметаллов и их соединений состоят из молекул, т. е. имеют молекулярное строение.
Химические свойства металлов и неметаллов
1. Химические свойства металлов определяются способностью отдавать свободные электроны с внешнего уровня. Они являются восстановителями. Взаимодействие идет с:
- неметаллами:
- +кислород O2 (кроме золота и металлов группы платины) → оксиды: 2Ca+ O2 → 2CaO;
- +галогены (F2, Cl2, Br2) → галогениды (фторид, хлорид, бромид и т.д.): Cu + Br2 → CuBr2;
- +азот, фосфор, сера, водород → нитриды, фосфиды, сульфиды, гидриды: 3Ca + N2 → Ca3N2.
- водой (только щелочные и щелочно-земельные металлы) → гидроксиды: 2Na + 2H2O → 2NaOH + H2↑;
- кислотами (металлы, стоящие в ряду активности до водорода) → соль: Mg + 2HCl → MgCl2 + H2↑;
- растворами солей менее активных металлов: Fe + CuSO4 → FeSO4 + Cu, при следующих условиях:
- соли, вступающие в реакцию и получающиеся в ходе нее, должны быть растворимы;
- металл вытесняет из соли другой металл, если находится левее в ряду активности;
- щелочные и щелочно-земельные металлы в данном случае будут вступать в реакцию с водой, а не с солью.
- оксидами (более активный металл вытесняет менее активный): Fe2O3 + 2Al → Al2O3 + 2Fe.
2. Химические свойства неметаллов обусловлены свободными электронами (от 3 до 7) на внешнем электронном уровне.
- окислительные свойства наиболее характерны (стремятся присоединять электроны) в реакциях с:
- металлами: O2+2Mg → 2MgO; S + 2Na → Na2S;
- неметаллами:
- кислород O2 (из галогенов реагирует только фтор): S + O2 → SO2;
- водород H2 (кроме кремния, фосфора и бора) : С + 2H2 → CH4;
- неметалл c меньшей электроотрицательностью: 3S + 2P → P2S3 (нагревание без доступа воздуха, сера — окислитель);
- солями (вытесняют менее активные неметаллы): Cl2 + 2NaBr → 2NaCl + Br2.
- восстановительные свойства (исключение: фтор F — всегда окислитель) в некоторых реакциях с:
- неметаллами, электроотрицательность которых ниже: C + O2→ CO2 (углерод — восстановитель);
- сложными веществами — окислителями (CuO, HNO3): S + 6HNO3 → H2SO4 + 6NO2↑ + 2H2O.
- и окислительные, и восстановительные свойства проявляют хлор, сера, фосфор, йод и бром в реакциях диспропорционирования:
- Cl20 + H2O → HCl-1 + HCl+1O;
- 3S0 + 6NaOH → 2Na2S-2 + Na2S+6O3 + 3H2O.
Химические свойства благородных газов
- плохо растворяются в воде и вступают в реакции с другими веществами только в специально созданных условиях;
- не горят; вытесняют кислород из воздуха, снижая его содержание до критически низких показателей, приводящих к смерти.
Строение и основные химические свойства сложных веществ
Сложные соединения имеют ионную или ковалентную связь между атомами.
- оснóвные + кислоты → соли: CaO + 2HCl → CaCl2 + H2O;
- кислотные + основания → соли: SO3 + 2NaOH → Na2SO4 + H2O;
- амфотерные реагируют и с кислотами, и с основаниями → соли:
ZnO + H2SO4 → ZnSO4 + H2О,
ZnO+ 2NaOH + H2O → Na2[Zn(OH)4].
Все основания реагируют с кислотами (реакция нейтрализации):
- KOH + 2HCl → KCl + H2O;
- 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O.
1. Щелочи взаимодействуют с:
- неметаллами: 6KOH + 3S → K2SO3 + 2K2S + 3H2O;
- кислотными оксидами: 2NaOH + NO2 → NaNO2 + NaNO3 + H2O.
2. Нерастворимые основания разлагаются при нагревании: Cu(OH)2 → CuO + H2O.
- + основания (реакция нейтрализации): 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O;
- + металлы, стоящие левее водорода в ряду активности: Mg + 2HCl → MgCl2 + H2↑;
- + основные и амфотерные оксиды: CaO + H2SO4 → CaSO4 + H2O; ZnO + H2SO4 → ZnSO4 + H2O;
- + соли: BaCl2 + H2SO4 → BaSO4 + 2HCl.
- + кислоты (сильные): Na2SiO3 + 2HCl → H2SiO3↓ + 2NaCl;
- + щёлочи, если образуется нерастворимое основание: FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl;
- + металлы: Zn + Pb(NO3)2 → Pb↓ + Zn(NO3)2;
- + соли при условии необратимости реакции: Na2CO3 + Ca(NO3)2 → CaCO3↓ + 2NaNO3.
Также о химических свойствах неорганических соединений можно почитать в статье «Классы неорганических соединений».
Источник