Структура льда, нановода
Кристаллическая структура льда напоминает структуру алмаза: каждая молекула Н2O окружена четырьмя ближайшими к ней молекулами, участвующих в формировании водородной связи и находящимися на одинаковых расстояниях от нее, равных 2,76 ангстрем и размещенных в вершинах правильного тетраэдра под углами, равными 109°28′ (рис. 34). В связи с низким координационным числом структура льда является сетчатой, что влияет на его невысокую плотность. Природный лёд обычно значительно чище, чем вода, т.к. растворимость веществ (кроме NH4F) во льде крайне низкая. При плавлении льда его кристаллическая структура частично сохраняется в жидкой воде.
Таблица. Некоторые данные о структурах модификаций льда
Длины водородных связей,
Углы О—О—О в тетраэдрах
Примечание. 1 A=10 -10 м.
Наиболее изученным является лёд I-й природной модификации, который распространён в природе в виде материкового, плавающего, подземного льда, а также в виде снега, инея и т.д. В отличие от природного льда льды II, III и V-й модификации могут существовать при очень низких температурах до —170°С. При нагревании до температуры —150°С образуется кубический лёд Ic. Лёд IV-й модификации является метастабильной фазой льда. Он образуется гораздо легче и особенно стабилен, если давлению подвергается тяжёлая вода. Кривая плавления льда V и VII исследована до давления 20 Гн/м 2 (200 тыс. кгс/см 2 ). При этом давлении лёд VII плавится при температуре 400°С. Лёд VIII является низкотемпературной упорядоченной формой льда VII. Лёд IX — метастабильная фаза, возникающая при переохлаждении льда III и по существу представляющая собой его низкотемпературную форму. Две последние модификации льда — XIII и XIV — открыли ученые из Оксфорда совсем недавно, в 2006 году. Предположение о том, что должны существовать кристаллы льда с моноклинной и ромбической решетками, было трудно подтвердить: вязкость воды при температуре –160°С очень высока, и собраться вместе молекулам переохлажденной воды в таком количестве, чтобы образовался зародыш кристалла, трудно. В лабораторных экспериментах этого удалось достичь с помощью катализатора — соляной кислоты, которая повысила подвижность молекул воды при низких температурах. В земной природе подобные модификации льда образовываться не могут, но они могут встречаться на замерзших спутниках других планет.
Значение льда для формирования и функционирования жизни трудно переоценить. Лёд оказывает большое влияние на условия обитания и жизнедеятельности растений и животных, на разные виды хозяйственной деятельности человека. Вследствие меньшей, чем у воды, плотности лёд образует на поверхности воды плавучий покров, предохраняющий реки и водоёмы от донного замерзания и сохраняющего жизнь подводному миру. Если бы плотность воды увеличивалась при замерзании, лед оказался бы тяжелее воды и начал тонуть, что привело бы к гибели всех живых существ в реках, озерах и океанах, которые замерзли бы целиком в толще льда, а Земля стала ледяной пустыней, что неизбежно привело бы к гибели всего живого на Земле.
Аналогично воде, кристалл льда способен хранить информацию. Группа ученых провела очень интересный эксперимент в Арктике. Было проведено зондирование во льду на глубине полкилометра. При этом отчётливо детектировались слои льда разных лет. Также был сделан изотопный анализ дейтерия и изотопов кислорода в составе Арктического льда. Согласно исследованиям, вода всегда успевала „запомнить” информацию соответствующего года. Оказалось, что самыми холодными были XV, конец XVII – го и начало XIX века. А самыми теплыми были 1550 и 1930 г.
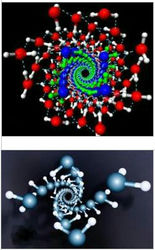
Но самое удивительное в структуре льда заключается в том, что молекулы воды при низких отрицательных температурах и высоких давлениях внутри нанотрубок могут кристаллизоваться в форме двойной спирали, похожей на ДНК. Это было доказано компьютерными экспериментами американских учёных под руководством Сяо Чэн Цзэна в Университете штата Небраска (США) (рис. 35).
Вода в моделируемом эксперименте «помещалась» в нанотрубки диаметром от 1,35 до 1,90 нм. под высоким давлением, варьирующимися в разных опытах от 10 до 40000 атмосфер. После этого задавали температуру, которая во всех экспериментах имела значение -23°C. Запас по сравнению с температурой замерзания воды делался в связи с тем, что с повышением давления температура плавления водяного льда понижается.
Рис. 35. Общий вид структуры воды в нанотрубках (изображение New Scientist)
Молекулы воды связаны между собой посредством водородных связей, расстояние между атомами кислорода и водорода равно 96 пм, а между двумя водородами — 150 пм. В твёрдом состоянии атом кислорода участвует в образовании двух водородных связей с соседними молекулами воды. При этом отдельные молекулы H2O соприкасаются друг с другом разноимёнными полюсами. Таким образом, образуются слои, в которых каждая молекула связана с тремя молекулами своего слоя и одной из соседнего. В результате, кристаллическая структура льда состоит из шестигранных «трубок» соединенных между собой, как пчелиные соты.
Согласно данным компьютерного моделирования, при диаметре трубки в 1,35 нм и давлении в 40000 атмосфер водородные связи искривились, приведя к образованию спирали с двойной стенкой. Внутренняя стенка этой структуры является скрученной в четверо спиралью, а внешняя состоит из четырёх двойных спиралей, похожих на структуру молекулы ДНК.
Последний факт накладывает отпечаток не только на эволюцию наших представлений о воде, но и эволюцию ранней жизни и самой молекулы ДНК. Если предположить, что в эпоху зарождения жизни криолитные глинистые породы имели форму нанотрубок, возникает вопрос — не могла ли вода, сорбированная в них служить структурной основой – матрицей для синтеза ДНК и считывания информации? Возможно, поэтому спиральная структура ДНК повторяет спиральную структуру воды в нанотрубках. Как сообщает журнал New Scientist, теперь нашим зарубежным коллегам предстоит подтвердить существование таких макромолекул воды в реальных экспериментальных условиях с использованием инфракрасной спектроскопии и спектроскопии нейтронного рассеяния.
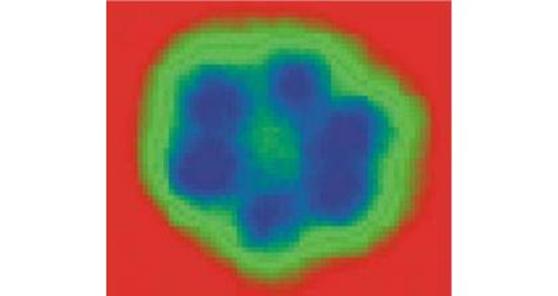
Такие исследования нанокристаллов льда были проведены в 2007 году Микаелидес из Центра нанотехнологий в Лондоне и Моргенштерн из университета им. Лейбница в Ганновере (рис. 36). Они охлаждали водяной пар над поверхностью металлической пластины, находящейся при температуре 5 градусов Кельвина. Вскоре с помощью сканирующего туннельного микроскопа на пластине удалось наблюдать гексамер (шесть соединенных между собой молекул воды) — мельчайшую снежинку. Это самый маленький из возможных кластеров льда. Ученые наблюдали также кластеры, содержащие семь, восемь и девять молекул.
Рис. 36. Изображение гексамера воды, полученное с помощью сканирующего туннельного микроскопа Размер гексамера в поперечнике — около 1 нм. Фото London Centre for Nanotechnology
Разработка технологии, позволившей получить изображение гексамера воды – само по себе важное научное достижение. Для наблюдения пришлось сократить зондирующий ток до минимума, что и позволило предохранить слабые связи между отдельными молекулами воды от разрушения вследствие процесса наблюдения. Помимо этого, в работе были использованы теоретические подходы квантовой механики. Комплексный подход дал впечатляющие результаты.
В отличие от кристаллического льда, где между всеми молекулами воды энергия связи одинакова, в нанокластерах есть чередование сильных и слабых связей (и соответствующих расстояний) между отдельными молекулами. Получены также важные результаты о способности молекул воды к распределению водородных связей и к их связи с поверхностью металла.
Теоретические анализы Опарина, эксперименты Миллера, Фокса и др. бесспорно доказывают, что в природе могут структурироваться органические молекулы из неорганических. Главным источником энергии в их экспериментах является тепло. В природе это солнечная радиация и энергия магмы. Другой очень существенный вывод – это, что зарождение жизни может произойти в щелочной среде. Во всех случаях наблюдается самоорганизация.
В XIX в. Пастьор обратил внимание, что в неживой природе молекулы являются симметрическими. А в живой природе наблюдается зеркальная ассиметрия молекул. Белки состоят из ориентированных влево аминокислот. Данное свойство определяется верчением молекулой равнины поляризации света. Как объяснить феномен?
Возможно, наличие ассиметрии в органических молекулах проявилось, когда открытая система, предшествувающая биосферу, находилась в крайне неравновесном критическом состоянии.
Произошел прыжкообразный эволюционный переход, что является характерной особенностью самоорганизации. Примером такого состояния являются эксперименты, где водные молекулы напоминают ДНК в нанотрубах. Переход из симметричных молекул неживой природы к ассиметричным биомолекулам живой может произойти на начальном этапе химической эволюции, как самоорганизация материи. Проф. Антонов доказал, что вода тоже является открытой системой и обменивается энергией и веществами с окружающей средой (проф. Антонов, 1992).
Такие экстремальные условия наблюдаются при вулканической деятельности,ются симметрическими. А в живой природе наблюдается зеркальная ассиметрия молекул. Белки состоят из ориентированных влево аминокислот. Данное свойство определяется вращением молекулой плоскости поляризации света. Как объяснить феномен? Возможно, наличие ассиметрии в органических молекулах проявилось, когда открытая система, предшествувающая биосферу, находилась в крайне неравновесном критическом состоянии. Такие экстремальные условия наблюдаются при вулканической деятельности, разрядах в атмосфере молодой Земли. Минеральная вода, взаимодействуюшая с карбонатом кальция, а также морская вода, являются благоприятным спектром для сохранения самоорганизующихся структур. Эффект Кирлиана в лабораторных условиях создает селективный разряд. При экспериментах Миллера тоже создаются неравновесные экстремальные условия с газовым разрядомПроизошел прыжкообразный эволюционный переход, что является характерной особенностью самоорганизации. Примером такого состояния являются эксперименты, где водные молекулы напоминают ДНК в нанотрубах. Переход из симметричных молекул неживой природы к ассиметричным биомолекулам живой может произойти на начальном этапе химической эволюции, как самоорганизация материи. Проф. Антонов доказал, что вода тоже является открытой системой и обменивается энергией и веществами с окружающей средой (проф. Антонов, 1992).глядит развитие Вольвокса. а) В течение первых пяти делений получается зародышевый диск из 32 (2 5 ) одинаковых клеток, этот диск сворачивается в сферу и из стенки родительской колонии выходит во внутреннее пространство колонии. b) Шестое деление клеток дает по две неравных по размеру клетки, одну большую и одну маленькую. с) Большие клетки делятся еще несколько раз на неравные по размеру клетки, а потом и вовсе прекращают деление, а маленькие клетки в это время продолжают обычное равномерное деление. d) На одном конце сферического зародыша появляется крестообразное отверстие. e) Это один из самых волнующих эпизодов взросления Вольвокса. Все клетки до того момента располагались жгутиками внутрь, так получилось, когда зародышевый диск сворачивался в сферу в начале развития, то есть был вывернут наизнанку. Теперь же зародыш должен вывернуться на лицевую сторону. И вот зародыш через появившееся отверстие начинает это выворачивание. f) После того как зародыш вывернулся до конца и все его жгутики торчат наружу, он считается совершеннолетним, после только увеличивается в размерах и вскоре покидает родительскую сферу. Из статьи D.L.Kirk (2005)
Развитие вольвокса имеет ряд удивительных особенностей самоорганизации, усложнения, сохранения и обмен информации живой материи. Однако самым любопытным фактом, является то, что такое важное эволюционное событие, как появление многоклеточности, на протяжение эволюции происходило неоднократно у разных групп животных и растений. Однако, рекордсменом, достойным книги Гиннеса, является семейство водорослей, к которому принадлежит вольвокс: многоклеточность в нем возникала независимо не менее 9 раз.
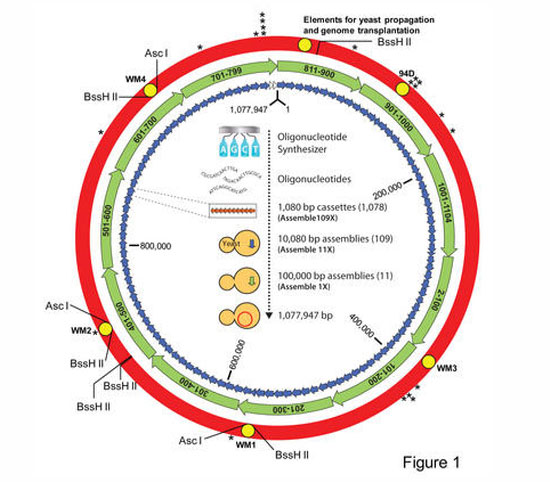
И наконец, в 2010 г. был осуществлён эксперимент американского учёного Крейга Вентера, который доказал способность передачи информации от одной клетки к другой. Он химическим путем синтезировал геном бактерии Mycoplasma mycoides и вставил его в клетку другого микроорганизма — Mycoplasma capricolum, из которой перед этим были удалены все гены. Полученный генный конструкт выжил, стал размножаться и повел себя как обычная бактерия Mycoplasma mycoides. Таким образом, впервые в мире удалось создать искусственный геном – своеобразный биокомпьютер и заставить живую клетку жить с этим генетическим кодом. Описание этой работы опубликовано в журнале Science.
Рис. Клетка с геномом другой клетки, Вентер
Цель эксперимента состояла в том, чтобы трансплантировать искусственно модифицированный геном одной из простейших бактерий (Mycoplasma mycoides) в клетки другой бактерии (Mycoplasma capricolum). Необычность этой манипуляции в том, что обмен геномами до сих пор был возможен между клетками разных типов – прокариотами и эукариотами, существенно отличающимися между собой по строению и представляющими собой две разные таксономические группы организмов. Вентеру удалось создать химерный гибридный организм из двух прокариот в отличие от природы, создавшей жизнь до уровня клетки из воды, атомов и молекул окружающей среды.
Таким образом, на основе многочисленных исследований, доказательств и модельных экспериментов человеческий ум стремится постичь загадку происхождения жизни, зародившейся в воде и покорившая все природные стихии.
Источник
Молекулы льда как расположены
Лёд — минерал с хим. формулой H2O , представляет собой воду в кристаллическом состоянии.
Химический состав льда: Н — 11,2%, О — 88,8%. Иногда содержит газообразные и твердые механические примеси.
В природе лёд представлен, главным образом, одной из нескольких кристаллических модификаций, устойчивой в интервале температур от 0 до 80°C, имеющей точку плавления 0°С. Известны 10 кристаллических модификаций льда и аморфный лёд. Наиболее изученным является лёд 1-й модификации — единственная модификация, обнаруженная в природе. Лёд встречается в природе в виде собственно льда (материкового, плавающего, подземного и др.), а также в виде снега, инея и т.д.
Смотрите так же:
СТРУКТУРА
Кристаллическая структура льда
Кристаллическая структура льда похожа на структуру алмаза: каждая молекула Н20 окружена четырьмя ближайшими к ней молекулами, находящимися на одинаковых расстояниях от нее, равных 2,76Α и размещенных в вершинах правильного тетраэдра. В связи с низким координационным числом структура льда является ажурной, что влияет на его плотность (0,917). Лед имеет гексагональную пространственную решётку и образуется путём замерзания воды при 0°С и атмосферном давлении. Решётка всех кристаллических модификаций льда имеет тетраэдрическое строение. Параметры элементарной ячейки льда (при t 0°С): а=0,45446 нм, с=0,73670 нм (с — удвоенное расстояние между смежными основными плоскостями). При понижении температуры они меняются крайне незначительно. Молекулы Н20 в решётке льда связаны между собой водородными связями. Подвижность атомов водорода в решётке льда значительно выше подвижности атомов кислорода, благодаря чему молекулы меняют своих соседей. При наличии значительных колебательных и вращательных движений молекул в решётке льда возникают трансляционные соскоки молекул из узла пространственной их связи с нарушением дальнейшей упорядоченности и образованием дислокаций. Этим объясняется проявление у льда специфических реологических свойств, характеризующих зависимость между необратимыми деформациями (течением) льда и вызвавшими их напряжениями (пластичность, вязкость, предел текучести, ползучесть и др.). В силу этих обстоятельств ледники текут аналогично сильно вязким жидкостям, и, таким образом, природные льды активно участвуют в круговороте воды на Земле. Кристаллы льда имеют относительно крупные размеры (поперечный размер от долей миллиметра до нескольких десятков сантиметров). Они характеризуются анизотропией коэффициента вязкости, величина которого может меняться на несколько порядков. Кристаллы способны к переориентации под действием нагрузок, что влияет на их метаморфизацию и скорости течения ледников.
СВОЙСТВА
Лёд бесцветен. В больших скоплениях он приобретает синеватый оттенок. Блеск стеклянный. Прозрачный. Спайности не имеет. Твердость 1,5. Хрупкий. Оптически положительный, показатель преломления очень низкий (n = 1,310, nm = 1,309). В природе известны 14 модификаций льда. Правда, все, кроме привычного нам льда, кристаллизующего в гексагональной сингонии и обозначающегося как лёд I , образуются в условиях экзотических — при очень низких температурах (порядка -110150 0С) и высоких давлениях, когда углы водородных связей в молекуле воды изменяются и образуются системы, отличные от гексагональной. Такие условия напоминают космические и не встречаются на Земле. Например, при температуре ниже –110 °С водяные пары выпадают на металлической пластине в виде октаэдров и кубиков размером в несколько нанометров — это так называемый кубический лед. Если температура чуть выше –110 °С, а концентрация пара очень мала, на пластине формируется слой исключительно плотного аморфного льда.
МОРФОЛОГИЯ
Пласты арктического льда
В природе лёд — очень распространенный минерал. В земной коре существует несколько разновидностей льда: речной, озёрный, морской, грунтовый, фирновый и глетчерный. Чаще он образует агрегатные скопления мелкокристаллических зерен. Известны также кристаллические образования льда, возникающие сублимационным путем, т. е. непосредственно из парообразного состояния. В этих случаях лед имеет вид скелетных кристаллов (снежинки) и агрегатов скелетного и дендритного роста (пещерный лёд, изморозь, иней и узоры на стекле). Крупные хорошо огранённые кристаллы встречаются, но очень редко. Н. Н. Стуловым описаны кристаллы льда северо-восточной части России, встреченные на глубине 55—60 м. от поверхности, имеющие изометрический и столбчатый облик, причем длина наибольшего кристалла равнялась 60 см., а диаметр его основания — 15 см. Из простых форм на кристаллах льда выявлены только грани гексагональной призмы (1120), гексагональной бипирамиды (1121) и пинакоида (0001).
Ледяные сталактиты, называемые в просторечии «сосульки», знакомы каждому. При перепадах температур около 0° в осенне-зимние сезоны они растут повсеместно на поверхности Земли при медленном замерзании (кристаллизации) стекающей и капающей воды. Они обычны также в ледяных пещерах.
Ледяные забереги представляют собой полосы ледяного покрова из льда, кристаллизующегося на границе вода-воздух вдоль краёв водоёмов и окаймляющие края луж, берега рек, озёр, прудов, водохранилищ, и тп. при незамерзающей остальной части водного пространства. При их полном срастании на поверхности водоёма образуется сплошной ледяной покров.
Лёд образует также параллельно-шестоватые агрегаты в виде волокнистых прожилков в пористых грунтах, а на их поверхности — ледяные антолиты.
ПРОИСХОЖДЕНИЕ
Лёд образуется в основном в водных бассейнах при понижении температуры воздуха. На поверхности воды при этом появляется ледяная каша, сложенная из иголочек льда. Снизу на неё нарастают длинные кристаллики льда, у которых оси симметрии шестого порядка размещаются перпендикулярно к поверхности корочки. Соотношения между кристаллами льда при разных условиях образования показаны на рис. Лед распространен всюду, где имеется влага и где температура опускается ниже 0° С. В некоторых районах грунтовый лед оттаивает только на незначительную глубину, ниже которой начинается вечная мерзлота. Это так называемые районы вечной мерзлоты; в областях распространения многолетнемерзлых пород в верхних слоях земной коры встречаются так называемые подземные льды, среди которых различают современный и ископаемый подземный лёд. Не менее 10% всей площади суши Земли покрывают ледники, слагающая их монолитная ледяная порода носит название ледниковый лёд. Ледниковый лёд образуется в основном из скопления снега в результате его уплотнения и преобразования. Ледниковый покров занимает около 75% площади Гренландии и почти всю Антарктиду; самая большая мощность ледников (4330 м.) – установлена близ станции Бэрд (Антарктида). В центральной Гренландии толщина льда достигает 3200 м.
Месторождения льда общеизвестны. В местностях с холодной долгой зимой и коротким летом, а также в высокогорных районах образуются ледяные пещеры со сталактитами и сталагмитами, среди которых наиболее интересными являются Кунгурская в Пермской области Приуралья, а также пещера Добшине в Словакии.
В результате замерзания морской воды образуется морской лёд. Характерными свойствами морского льда являются солёность и пористость, которые определяют диапазон его плотности от 0,85 до 0,94 г/см 3 . Из-за такой малой плотности льдины возвышаются над поверхностью воды на 1/7-1/10 своей толщины. Морской лёд начинает таять при температуре выше -2,3° С; он более эластичен и труднее поддается раздроблению на части, чем лёд пресноводный.
ПРИМЕНЕНИЕ
В конце 1980-х годов лаборатория Аргонн разработала технологию изготовления ледяной гидросмеси (Ice Slurry), способной свободно течь по трубам различного диаметра, не собираясь в ледяные наросты, не слипаясь и не забивая системы охлаждения. Солёная водяная суспензия состояла из множества очень мелких ледяных кристалликов округлой формы. Благодаря этому сохраняется подвижность воды и, одновременно, с точки зрения теплотехники она представляет собой лёд, который в 5—7 раз эффективнее простой холодной воды в системах охлаждения зданий. Кроме того, такие смеси перспективны для медицины. Опыты на животных показали, что микрокристаллы смеси льда прекрасно проходят в довольно мелкие кровеносные сосуды и не повреждают клетки. «Ледяная кровь» удлиняет время, в течение которого можно спасти пострадавшего. Скажем, при остановке сердца это время удлиняется, по осторожным оценкам, с 10—15 до 30—45 минут.
Использование льда в качестве конструкционного материала широко распространено в приполярных регионах для строительства жилищ — иглу. Лёд входит в состав предложенного Д. Пайком материала Пайкерит, из которого предлагалось сделать самый большой в мире авианосец.
Источник