IT News
Last update Вс, 29 Янв 2017 11pm
Почему лед не нагревается во время таяния?
Если лед поместить в сосуд и поставить его над работающей горелкой, сосуд нагреется и лед начнет таять. Однако до тех пор, пока весь лед не превратится в жидкость, температура воды не поднимется выше 0°С (32°F), вне зависимости от степени разогрева плиты. Это происходит из-за того, что вся подводимая ко льду теплота идет на преодоление физических сил, связывающих между собой его молекулы.
У льда молекулы воды удерживаются вместе межмолекулярными связями, формирующимися между атомом водорода (показан синим цветом) одной молекулы и атомом кислорода (показан красным цветом) другой. Результирующая гексагональная кристаллическая структура имеет довольно высокую прочность. При 0°С молекулы движутся настолько быстро, что связи ослабевают. Часть межмолекулярных связей разрывается, позволяя молекулам воды покидать лед с образованием жидкости. Такой процесс называется фазовым переходом (вода переходит из твердой фазы в жидкую), а температура, при которой он протекает, называется точкой плавления.
Для разрушения связей, позволяющих воде находиться в твердом состоянии, необходима энергия, причем в очень большом количестве, поэтому вся теплота, выделяемая горелкой, идет на разрывание этих связей, а не на увеличение температуры льда. Теплота, необходимая для завершения описанного выше фазового превращения, называется скрытой теплотой плавления или теплотой фазового перехода, так как эта теплота не приводит к росту температуры. Только после того, как последние связи будут разрушены и весь лед расплавится, температура воды начнет увеличиваться и станет выше 0°С.
Как происходит таяние льда
- У льда молекулы воды движутся так медленно, что всегда сохраняют связь друг с другом, образуя твердое тело. Когда ко льду подводится теплота (на рисунке справа показана в виде желтых шариков), молекулы воды приобретают дополнительную энергию и движутся быстрее, однако все еще связанные вместе в виде льда.
- Если подвод теплоты продолжается, молекулы воды, находящиеся на поверхности льда, увеличивают скорость своих колебательных движений, разрывая межмолекулярные связи, удерживавшие их раньше на месте. Эти молекулы покидают лед и образуют жидкую фазу воды. Дальнейший подвод теплоты приводит к разрушению оставшихся межмолекулярных связей и постепенному таянию льда.
- Продолжающийся подвод теплоты в конце концов дает последним из молекул замерзшей воды достаточно энергии для преодоления межмолекулярных связей, удерживавших их вместе в виде льда. Вся вода теперь стала жидкостью.
Лед, вода и температура
При подводе ко льду теплоты (рисунок слева) сначала увеличивается его температура. Однако при 0°С (32°F) рост температуры прекращается и наступает фазовый переход: лед начинает таять. Как показывает голубая кривая на графике, дополнительный подвод теплоты приводит к дальнейшему таянию льда, не увеличивая температуру воды. Только после того как весь лед перейдет в жидкое состояние (рисунок над текстом), дополнительный подвод теплоты приводит к увеличению температуры воды.
Источник
то от чего тает лёд
Почему тает лед?
Иногда так хочется, чтоб зима не заканчивалась, на улице постоянно был снег и лед, на котором так интересно кататься, но приходит весна и на улице пропадает все зимнее одеяние и многие дети остаются в недоумении, куда ушла зима и почему тает лед?
Многие взрослые готовы сегодня Вам ответить на этот вопрос достаточно легко, но не всегда можно понять, почему в природе происходит то или иное явление.
Лед – это вода, которая приобрела твердое состояние под действием холодной температуры. Кроме того что вода может замерзать, она может осуществлять и обратное действие, то есть таять. Этот процесс происходит по-разному в зависимости от температуры воздуха и внешних условий. Нужно помнить, что лед это не твердое тело в принципе, поэтому это его не обычное состояние. Для того чтоб вода растаяла, необходимо положить лед в теплое место. С приходом весны на улице постепенно повышается температура воздуха и со временем весь лед и снег превращается в ручьи и лужи, то есть воду. Таянье происходит уже при отметке +1 и выше, поэтому если на термометре Вы видите положительное значение, а на улице в это время снег или гололед, можно ожидать того, что к концу дня лед начнет таять и превращаться в воду.
Для того чтоб доказать эффект существования процесса таянья попробуйте взять лед в руку. Известно, что температура тела человека в обычном состоянии задерживается на отметке +36оС, поэтому лед в руках непременно начнет таять в тот же момент, как только Вы положите кусочек льда в ладошку, при этом в руке появится вода, это будет доказательством того, что лед – это не просто тело, а вода, которая замерзла. Вода может приобретать разное состояние, но при этом она не исчезает в никуда. Она может превращаться в лед или пар, но при этом легко возвращается в предыдущее состояние при малейших усилиях человека.
[ссылка заблокирована по решению администрации проекта]
Источник
Лед тает
В этой статье блога Вольных Ледорубов речь пойдет о природе таяния льда. Почему лед тает, каким образом, при каких условиях и с какой скоростью?
Как известно, вода в окружающей нас среде находится в трех ипостасях – в виде жидкости, в виде пара, и в виде твердого тела (иначе говоря, льда), при этом вода может свободно переходить из твердого агрегатного состояния в жидкое, из жидкого в газообразное, и наоборот, всегда возвращаясь к исходным свойствам.
Нуль градусов по шкале Цельсия (0°С), при условии нормального атмосферного давления в 1 атмосферу (760 мм ртутного столба), является температурным значением фазового перехода воды из жидкого состояния в твердое (кристаллы льда) и, наоборот, из твердого в жидкое. Получается, что при постоянной нулевой температуре вода может быть как льдом, так и жидкостью, а вопрос кристаллизации или таяния заключается лишь в том, в какой начальной фазе состоит вода и какое на нее оказывается воздействие. В этой температурной точке лед продолжает оставаться льдом, а жидкость – жидкостью, если, соответственно, температура окружающего воздуха не поднимется выше нулевой отметки или не опустится ниже нее. В противном случае происходит теплообмен. То есть, нагревание льда при нуле градусов приводит к тому, что его температура уже не повышается – затраченное тепло уходит на разрушение кристаллической структуры льда, а после того, как весь лед растает и станет жидкостью, дальнейшее нагревание обусловит повышение температуры воды. В процессе замерзания дело обстоит ровно наоборот – с понижением окружающей температуры ниже нуля вода кристаллизуется, высвобождая при этом то количество энергии (тепла), которое необходимо для таяния того же объема льда.

Говоря о таянии льда или кристаллизации жидкой воды, стоит учесть некоторые существенные факторы, влияющие на эти процессы.
Как было уже отмечено, и для первого, и для второго фазового перехода важным условием является давление. Для большинства веществ характерно то, что при фазовом переходе увеличение давления способствует увеличению температуры нагревания. Высокое давление приводит к тому, что атомы вещества начинают уплотняться, соответственно кристаллическая решетка сжимается, следовательно, на ее разрушение требуется больше энергии. Однако в случае с водой зависимость температуры от давления выглядит иначе. Вода, замерзая, превращается в твердое тело (лед), но в отличие от многих веществ, при затвердевании она не уменьшается, а, наоборот, увеличивается в объеме примерно на 9%. Плотность льда меньше плотности воды в жидком виде, при 0°С у льда она составляет 916.7 кг/м3, а у воды – 999.8 кг/м3 (вот почему лед и не тонет в воде), а значит, увеличение давления способствует ускорению перехода воды из твердого состояния в жидкое, что в свою очередь приводит к снижению температуры плавления льда. Например, чтобы снизить температуру плавления льда на 1°С нужно увеличить давление боле чем на 100 кгс/см2 (килограмм-сила/кв.см) или 10 МПа (мегапаскалей).
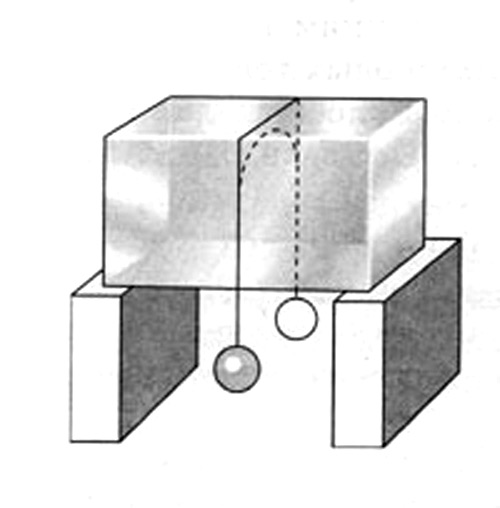
Зависимость температуры плавления льда от давления
Наглядно зависимость температуры плавления льда от давления можно увидеть на опыте. Через ледяной блок перекидывается нейлоновая нить, а к концам нити привязываются грузы; под давлением нити лед подтаивает, нить опускается, а образовавшаяся вода следом за нитью обратно замерзает. Таким образом, нить постепенно проходит сквозь лед, а сам ледяной блок в то же время остается целым.
Важным условием для образования льда является содержание в воде мельчайших взвесей, которые будут в данном случае являться ядрами ледяных кристаллов (о формировании ледяных кристаллов Вы также можете прочесть в статье « Микроледяные скульптуры »).
Дистиллированная же вода, очищенная от всяких примесей, может оставаться жидкостью и при отрицательной температуре, так как молекулам воды не за что будет зацепиться, чтобы создать кристаллическую решетку, но только в том случае, когда на воду не оказывается воздействие. А если же, к примеру, в сосуд с очищенной водой бросить кусок льда или бутылку с дистиллятом встряхнуть, процесс кристаллизации будет мгновенным, и за несколько секунд вода превратится в лед, благодаря пузырькам воздуха, микрочастицам, попавшим в воду, неровностям на поверхности сосуда.
Дистиллированная вода находясь на больших высотах в виде мельчайших капелек не замерзает даже при очень низких температурах, от -30 °С и ниже.
На фазовые переходы воды влияет также степень ее солености. Морская вода, в отличие от пресной, замерзает всегда при температуре ниже 0°С. Различие температур ее замерзания зависит от концентрации в ней солей, например, при 20%-ной солености температура замерзания составляет около -1°С, а при 40%-ной – чуть выше 2°С.
Концентрация соли снижает и температуру плавления льда. Мы часто с вами видели, как заледенелые проезжие части и пешеходные дорожки посыпали солью. Так вот, соль соединяясь с крупинками верхнего слоя льда, благодаря механическому воздействию, оказываемому нашими ногами и колесами автотранспорта, а также солнечным лучам и ветру, вызывающим подтаивание ледяной корки, образует своего рода смесь. Температура плавления смесей всегда ниже, чем температура плавления отдельных веществ, поэтому лед на дорогах начинает таять незамедлительно. При таянии образуется соленый водный раствор, который помогает растопить лед дальше.
Источник
Почему лед тает физика
Кружок « Мы и физика”
(«««`+`@` («««««` 33 True 0 («««`%«` («««««` 3 452 453 455 451 4 509 508 3 452 True («««`!«` («««««` 134217728 134217735 False False False 134217735 0 1 True True False 134217732 36576 36576 36576 36576 36576 36576 36576 36576 True 0 -1 453 True («««`*`@` («««««` 134217728 134217735 False False False 134217728 0 1 True True False 134217732 36576 36576 36576 36576 36576 36576 36576 36576 -1 455 True («««`+`@` («««««` 202 134217735 134217735 False False False 134217728 0 1 True True False 134217732 0 0 0 0 72390 36576 36576 36576 36576 1 -1 False 1 1 
| Кружок « Мы и физика », средняя школа № 99 |
True («$««*«` («««««` 31 True 2 1924560 720000
| Адрес основного места работы улица Молодова 12 |
True True («««!P«` («««««` 30 2686050 468000
| Кто ищет, тот всегда найдет! |
True True («««`G!P` («««««` 29 2 2686050 1057275
Как тает лед—быстро или медленно? |
True («««!G!0` («««««` 28 True 2 1600200 371475
| Телефон: 42- 47-07; 42-42-75. |
True True («««!)!0` («««««` 26 True 5020560 5364000
| Цель: нужно узнать и объяснить, какой лед растает быстрее: тот, который обернут в фольгу, бумагу или вату. Для этого опыта мы приготовили три одинаковых кусочка льда массой приблизительно 20 г и оставили в комнате. Наши наблюдения показали, что через 1 час полностью растаял лед, завернутый в фольгу; еще через 10 минут растаял лед, завернутый в бумагу; самый долговременный лед, который не растаял,- это обернутый ватой. У воздуха плохая теплопроводность, поэтому этот лед растаял позже всех остальных. Бумага — это теплоизолятор, но все же ее теплопроводность больше, чем у ваты, поэтому лед, обернутый в бумагу, растаял вторым. Фольга состоит из алюминия, а алюминий – это металл, а мы знаем, что металлы быстрее всего нагреваются, т.к. у них высокая теплопроводность, поэтому в фольге лед быстрее всего растаял. Между волокнами ваты содержится много воздуха. Различные тела имеют неодинаковую теплопроводность, у металлов она выше, у стекла меньше, а у дерева еще меньше. Очень плохим проводником тепла является воздух. Вавилова Валерия и Бахерева Оксана , ученицы 8 А класса. Экспериментальные исследования и решение задач по теме « Тепловые явления » Источник |