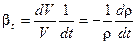- Теплота сублимации льда при температуре таблица
- Плотность льда и снега, теплопроводность, теплоемкость льда
- Плотность, теплопроводность и теплоемкость льда в зависимости от температуры
- Теплофизические свойства льда и снега
- Давление насыщенного пара льда
- Физико-механические и теплофизические свойства льда и шуги
- Теплота сублимации льда при температуре таблица
Теплота сублимации льда при температуре таблица
УДАРНАЯ ВЯЗКОСТЬ (УДЕЛЬНАЯ ЭНЕРГИЯ РАЗРУШЕНИЯ ЛЬДА). Механическая характеристика сопротивления льда ударной нагрузке, следствием которой является местное смятие и раздробление определенного, зависящего от энергии удара объема льда вблизи зоны контакта. Ударная вязкость может оцениваться работой разрушения надрезанного образца при ударном изгибе на маятниковом копре. Выражается в Дж/м 2 и определяется как отношение работы к площади поперечного сечения в месте надреза. Удельная энергия разрушения оценивается по энергии удара, отнесенной к объему разрушенного льда (Дж/м 3 ) или к массе раздробленного льда (Дж/кг).
В инженерных расчетах ударных нагрузок и воздействия льда на гидротехнические сооружения согласно строительным нормам и правилам (СНиП) в качестве прочностной характеристики применяют термин прочность льда на раздробление (с учетом местного смятия). Значение этой характеристики, в зависимости от отношения ширины сооружения к толщине взаимодействующей с ним льдины, выбирают в 0,5—2,5 раза больше предела прочности
УДЕЛЬНАЯ ТЕПЛОТА ВОЗГОНКИ ЛЬДА. Количество теплоты, которое необходимо сообщить льду, чтобы перевести его в пар при неизменной температуре.
УДЕЛЬНАЯ ТЕПЛОТА ПЛАВЛЕНИЯ ЛЬДА. Количество теплоты, затрачиваемое на переход единицы массы льда при его фазовом превращении из кристаллического состояния в жидкое при температуре плавления. При 0 °С и нормальном атмосферном давлении для чистого льда удельная теплота плавления льда равна 333,5 кДж/кг. Это значение совпадает с удельной теплотой кристаллизации пресной воды.
Для морского льда пользуются термином эффективная теплота плавления, под которым понимают некоторую характеристику эффективного тепла, необходимого для расплавления единицы массы соленого льда, взятого при некоторой температуре. Эффективная теплота плавления льда с увеличением его солености резко уменьшается.
УДЕЛЬНАЯ ТЕПЛОТА СУБЛИМАЦИИ ВОДЯНОГО ПАРА. Количество теплоты, которое необходимо сообщить пару, чтобы перевести его в лед при неизменной температуре.
УДЕЛЬНАЯ ЭНЕРГИЯ РАЗРУШЕНИЯ ЛЬДА. См. ударная вязкость.
УПРУГОСТЬ ЛЬДА. Свойство льда, характеризующее его способность сопротивляться изменению объема и формы вследствие возникновения во льду механических напряжений, вызванных внешней нагрузкой, объемными силами, температурными градиентами и другими источниками напряжений при условии соблюдения закона Гука.
УСЛОВНО-МГНОВЕННАЯ ПРОЧНОСТЬ ЛЬДА. См. хрупкая прочность льда.
УСТОЙЧИВОСТЬ ЛЕДЯНОГО ПОКРОВА. Способность ледяного покрова сохранять во времени свою пространственную структуру и его характеристики.
УСТОЙЧИВОСТЬ НАПРАВЛЕНИЯ ДРЕЙФА ЛЬДОВ. Степень сохранения системой дрейфа льдов своего направления, которая оценивается отношением модуля вектора средней скорости W к средней скалярной скорости W*
Источник
Плотность льда и снега, теплопроводность, теплоемкость льда
Плотность, теплопроводность и теплоемкость льда в зависимости от температуры
В таблице приведены значения плотности, теплопроводности, удельной теплоемкости льда в зависимости от температуры в интервале от 0 до -100°С.
По данным таблицы видно, что с понижением температуры удельная теплоемкость льда уменьшается, а теплопроводность и плотность льда, напротив, растут. Например, при температуре 0°С плотность льда имеет значение 916,2 кг/м 3 , а при температуре минус 100°С его плотность становится равной 925,7 кг/м 3 .
Значение удельной теплоемкости льда при 0°С составляет 2050 Дж/(кг·град). При снижении температуры льда с -5 до -100°С его удельная теплоемкость снижается в 1,45 раза. Теплоемкость льда в два раза меньше значения этой величины у воды.
Теплопроводность льда при понижении его температуры с 0 до минус 100°С увеличивается с 2,22 до 3,48 Вт/(м·град). Лед более теплопроводен, чем вода — он может проводить в 4 раза больше тепла при одинаковых граничных условиях.
Следует отметить, что плотность льда меньше плотности воды, однако с понижением температуры плотность льда растет и при приближении к абсолютному нулю температуры плотность льда становится близка к величине плотности воды.
| Температура, °С | Плотность, кг/м 3 | Теплопроводность, Вт/(м·град) | Теплоемкость, Дж/(кг·град) |
|---|---|---|---|
| 0.01 (Вода) | 999,8 | 0,56 | 4212 |
| 0 | 916,2 | 2,22 | 2050 |
| -5 | 917,5 | 2,25 | 2027 |
| -10 | 918,9 | 2,30 | 2000 |
| -15 | 919,4 | 2,34 | 1972 |
| -20 | 919,4 | 2,39 | 1943 |
| -25 | 919,6 | 2,45 | 1913 |
| -30 | 920,0 | 2,50 | 1882 |
| -35 | 920,4 | 2,57 | 1851 |
| -40 | 920,8 | 2,63 | 1818 |
| -50 | 921,6 | 2,76 | 1751 |
| -60 | 922,4 | 2,90 | 1681 |
| -70 | 923,3 | 3,05 | 1609 |
| -80 | 924,1 | 3,19 | 1536 |
| -90 | 924,9 | 3,34 | 1463 |
| -100 | 925,7 | 3,48 | 1389 |
Теплофизические свойства льда и снега
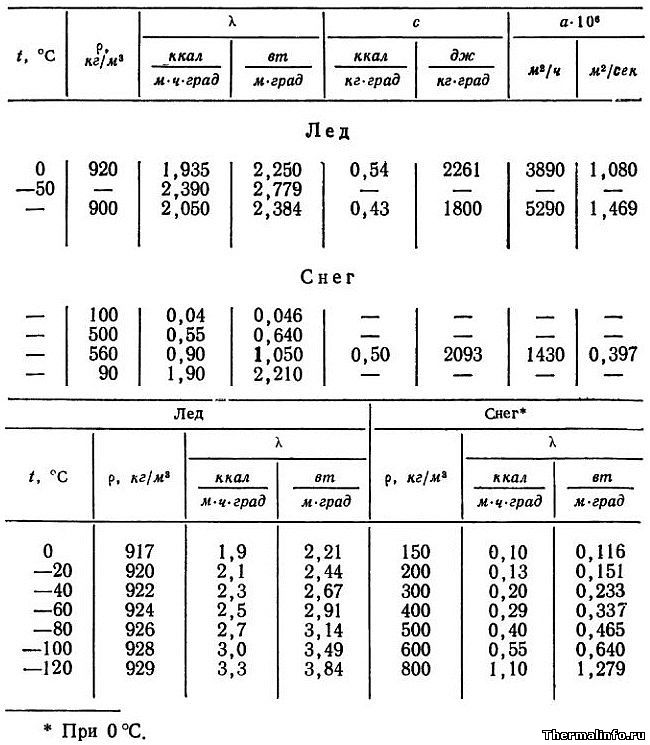
В таблице представлены следующие свойства льда и снега:
- плотность льда, кг/м 3 ;
- теплопроводность льда и снега, ккал/(м·час·град) и Вт/(м·град);
- удельная массовая теплоемкость льда, ккал/(кг·град) и Дж/кг·град);
- коэффициент температуропроводности, м 2 /час и м 2 /сек.
Свойства льда и снега представлены в зависимости от температуры в интервале: для льда от 0 до -120°С; для снега от 0 до -50°С в зависимости от уплотненности (плотности). Температуропроводность льда и снега в таблице приведена с множителем 10 6 . Например, температуропроводность льда при температуре 0°С равна 1,08·10 -6 м 2 /с.
Давление насыщенного пара льда
В таблице приведены значения давления насыщенного пара льда при сублимации (переход льда в пар, миную жидкую фазу) в зависимости от температуры в интервале от 0,01 до -80°С. Из таблицы видно, что с понижением температуры льда давление его насыщенного пара снижается.
Источник
Физико-механические и теплофизические свойства льда и шуги
Плотность льда, образовавшегося при кристаллизации пресной воды при 0°С и нормальном давлении, составляет в среднем 917 кг/м 3 . Следовательно, плотность пресноводного льда меньше плотности воды. Плотность льда зависит от его структуры, температуры и в большей степени от его пористости (во льду рек и водоемов почти всегда наблюдаются пузырьки воздуха).
С понижением температуры плотность льда увеличивается, а объем уменьшается. В зависимости от температуры плотность и удельный объем льда можно рассчитать по формулам Вейнберга:
ρ = 917 (1 — 0,000158t)(1 — n); (2.33)
где п — пористость льда.
Из (2.33) следует, что, зная плотность льда (rл,n=0.=917кг/м 3 ), можно определить его пористость
Плотность льда, образовавшегося в результате замерзания соленой воды(морской или озерной), зависит не только от его температуры и количества воздушных пузырьков в нем, но еще и от содержания солей в прослойках между кристаллами льда и от количества в этих прослойках рассола. И то и другое зависит от быстроты замерзания и от возраста льда. Старый морской лед имеет иное распределение солености по глубине, чем молодой. В морском льду рассол стекает вниз по неизбежным во льду трещинам, вследствие чего соленость его непрерывно изменяется во времени. Соленость льда всегда меньше солености воды, из которой он образовался.
Плотность морского льда увеличивается по мере увеличения солености воды и уменьшается с увеличением содержания воздушных пузырьков.
Расширение (сжатие) характеризуется коэффициентом объемного расширения, который равен отношению относительного изменения объема вещества V к изменению температуры t и определяется по формуле
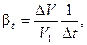
Коэффициент объемного расширения (сжатия) льда βt можно принять с достаточно высокой точностью постоянным и равным
0,158·10 -3 °С -1 . Коэффициент линейного расширения (сжатия) соответственно равен at = βt/3 = 0,053·10 -3 °С -1 .
Лед течет при напряжениях в ледяном покрове P > 5·10 4 Па. Характеристикой его текучести является коэффициент вязкости μ. Этот коэффициент определяется в зависимости от температуры льда по формулам:
при t ≥ -20°С
μ = (11,6 – 0,978t +0,293t 2 ) 10 11 , (2.35)
при t 11 , (2.36)
где t — средняя температура слоя льда.
ДЛЯ ВОДЫ при t = 0 0 μ = 1,793·10 3 Па·с
Коэффициент μ также сильно зависит от структуры льда, характера нагрузки и продолжительности ее приложения.
Плавление льда при постоянном внешнем давлении протекает при определенной температуре, называемой температурой плавления — tпл.
Температура плавления льда определяется давлением, при котором он находится; она понижается с повышением давления (рис. 2.2). Зависимость ее от давления описывается уравнением Клапейрона—Клаузиуса, а также может быть представлена следующей формулой:

При давлении до 10 7 Па эту зависимость можно заменить линейной:
Рис. 2.2. Ход температуры во льду во времени при подводе к нему теплоты [8]
1 — 2 — нагревание льда; 2 — 3 — плавление льда: 3 — 4— нагревание воды; tпл —температура плавления льда.
Плавление льда при атмосферном давлении происходит при температуре 0,01°С (в практических расчетах принимают 0°С).Количество теплоты, которое необходимо сообщить 1 кг льда, находящемуся при температуре плавления, для превращения его в воду, называют удельной теплотой плавления Lпл. Удельная теплота плавления пресноводного льда при нормальных условиях равна удельной теплоте кристаллизации воды 33,3·10 4 Дж/кг (п. 2.1).
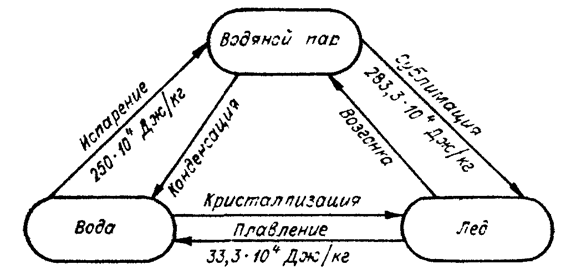
Удельная теплота сублимации (возгонки) льда (рис. 2.3) равна сумме удельной теплоты плавления льда и удельной теплоты испарения воды; при 0°С она равна
Lвоз = 33,3·10 4 + 250·10 4 = 283,3·10 4 Дж/кг.
Коэффициент теплопроводности льда λ принимают в среднем равным 2,24Вт/(м·°С). С повышением температуры λуменьшается незначительно и линейно.
Удельную теплоемкость льда вычисляют по формуле Б. П. Вейнберга:
c = 2,12 (1 + 0,0037t). (2.39)
При t=0°С теплоемкость льда c = 2,12 кДж/(кг·°С).
Рис. 2.3. Схема изменения агрегатного состояния воды [8]
Таблица 2.4
Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Студалл.Орг (0.008 сек.)
Источник
Теплота сублимации льда при температуре таблица
Из физики известно, что понятия «холод» и «теплота» условны, так как их физическая природа одинакова. Теплота — это один из видов энергии, который может быть преобразован в ее другие виды, и наоборот. Теплота может переходить от одного вещества (тела*) к другому лишь при наличии разности температур между ними.Вещества находятся в одном из трех (основных) фазовых (агрегатных) состояний — твердом, жидком или газообразном — в зависимости от окружающих условий (давления и температуры) и могут переходить из одного состояния в другое при подводе или отводе теплоты, вызывающей изменение строения вещества.Твердая фаза — агрегатное состояние вещества, характеризуемое жесткой молекулярной структурой. Твердое тело сохраняет свою форму и размеры, практически не сжимается.Жидкая фаза — агрегатное состояние вещества, молекулы которого, обладающие большей энергией, чем молекулы твердого тела, не так плотно соединены друг с другом. Это позволяет им более легко преодолевать силы взаимного притяжения. Жидкость практически не сжимается, сохраняет свой объем. Наиболее характерная особенность жидкости — текучесть, благодаря которой она принимает форму сосуда, в котором находится.Газовая или паровая фаза — агрегатное состояние вещества, молекулы которого, обладающие большей энергией, чем молекулы жидкости, не связаны силами взаимного притяжения и движутся свободно. Газ легко сжимается и заполняет весь объем сосуда, в котором находится.* В физике под термином «тело». Понимают любое вещество независимо от его агрегатного состояния. В холодильной технике обычно имеют дело с веществами в жидком или газообразном состоянии.Пар отличается от газа тем, что его состояние ближе к жидкому состоянию. Газ — это сильно перегретый пар. В парокомпрессионных холодильных машинах рабочее вещество обычно находится в жидком и парообразном состоянии, в отличие от так называемых газовых холодильных машин, в которых рабочее вещество — газ — не меняет своего агрегатного состояния.Если температура вещества выше температуры окружающей среды (воздуха, воды и пр.), то его называют горячим (теплым или нагретым). Самопроизвольное понижение температуры вещества до температуры окружающей среды называют естественным охлаждением.Понижение температуры вещества ниже температуры окружающей среды возможно путем искусственного охлаждения, а само вещество, температура которого ниже температуры окружающей среды, называют холодным.Таким образом, исходя из относительности понятий холода и теплоты, можно дать следующее определение: холод — это теплота, отводимая от вещества, температура которого ниже температуры окружающей среды.По температурному уровню различают области (рис. 1): умеренного холода — от температуры окружающей среды (условно 20°С) до —120°С — и глубокого холода — от —120 °С до абсолютного нуля (—273,15 °С).
Пар отличается от газа тем, что его состояние ближе к жидкому состоянию. Газ — это сильно перегретый пар. В парокомпрессионных холодильных машинах рабочее вещество обычно находится в жидком и парообразном состоянии, в отличие от так называемых газовых холодильных машин, в которых рабочее вещество — газ — не меняет своего агрегатного состояния.
Если температура вещества выше температуры окружающей среды (воздуха, воды и пр.), то его называют горячим (теплым или нагретым). Самопроизвольное понижение температуры вещества до температуры окружающей среды называют естественным охлаждением.
Понижение температуры вещества ниже температуры окружающей среды возможно путем искусственного охлаждения, а само вещество, температура которого ниже температуры окружающей среды, называют холодным.
Таким образом, исходя из относительности понятий холода и теплоты, можно дать следующее определение: холод — это теплота, отводимая от вещества, температура которого ниже температуры окружающей среды.
По температурному уровню различают области (рис. 1): умеренного холода — от температуры окружающей среды (условно 20°С) до -120°С — и глубокого холода — от -120 °С до абсолютного нуля (-273,15 °С).
Искусственное охлаждение можно осуществлять двумя способами:
- с помощью другого вещества с более низкой температурой за счет отвода теплоты, чаще всего при изменении его агрегатного состояния;
- с помощью охлаждающих устройств, холодильных машин и установок, которые составляют специализированную область техники, называемую холодильной техникой.
Прежде чем перейти к более подробному рассмотрению способов искусственного охлаждения, остановимся еще на некоторых понятиях и определениях, без усвоения которых невозможно изучение основ холодильной техники.
Количество теплоты Q измеряют в джоулях (Дж) или килоджоулях (кДж).
Тепловой поток, тоже Q,- это количество теплоты, отводимое (подводимое) от вещества (к веществу) в 1 с. Следовательно, тепловой поток выражают в джоулях в секунду (Дж/с) или в килоджоулях в секунду (кДж/с). Но 1Дж/с=1Вт, а 1 кДж/с=1 кВт, т. е. тепловой поток как один из видов энергии выражают в тех же единицах, что и мощность.
Удельная теплоемкость с — это количество теплоты в Дж (кДж), которое необходимо отвести (подвести) от вещества (к веществу) массой 1 кг, чтобы понизить (повысить) его температуру на 1 °С (или 1 К — Кельвин). Эта величина зависит от температуры вещества и его агрегатного состояния.
В практических расчетах можно принимать следующие значения удельной теплоемкости:
для воды — 4,19 кДж/( кг*К ), глицерина — 2,26, водного льда — 2,095, стали — 0,425, воздуха при давлении 0,1 МПа (760 мм рт. ст.) — 1 кДж/( кг-К ).
При отводе (подводе) теплоты переход через определенный температурный предел вызывает изменение агрегатного состояния.
Так, при дальнейшем отводе теплоты от воды, когда ее температура уже снизилась до О°С, она замерзает, а при дальнейшем подводе теплоты, когда температура поднялась до 100°С, вода закипает.
Обычно теплоту, вызывающую изменение только температуры (без изменения агрегатного состояния) называют «сухой». Ее количество, необходимое для понижения (повышения) температуры вещества массой М от начальной температуры t1 до конечной t2, определяют по формуле:
Q=Mc(t1- t2).
Физические принципы получения низких температур
1. Охлаждение за счет фазовых превращений. При достижении твердым телом температуры плавления дальнейшего повышения его температуры не происходит, а подводимая (или отводимая) теплота тратится на изменение агрегатного состояния — превращение твердого тела в жидкость (при отводе теплоты — из жидкости в твердое тело).
Температура плавления (затвердевания) зависит от вида вещества и давления окружающей среды.
При атмосферном давлении (760 мм рт. ст.) температура плавления водного льда равна О°С. Количество теплоты, необходимое для превращения 1 кг льда в воду (или наоборот), называется скрытой или удельной теплотой плавления r.
Для водного льда r=335 кДж/кг.
Количество теплоты, необходимое для превращения льда массой М в воду, определяют по формуле:
Q=Mr.
Из сказанного следует, что одним из способов искусственного охлаждения является отвод теплоты за счет плавления вещества в твердом состоянии при низкой температуре.
На практике этот способ давно и широко применяют, осуществляя охлаждение с помощью заготовленного зимой с использованием природного холода водного льда или с помощью замороженной в ледогенераторах с использованием холодильных машин воды.
При плавлении чистого водного льда температуру охлаждаемого вещества можно понизить до О °С. Для достижения более низких температур используют льдосоляные смеси. В этом случае температура и скрытая теплота плавления зависят от вида соли и ее содержания в смеси. При содержании в смеси 22,4 % хлористого натрия температура плавления льдосоляной смеси равна -21,2°С, а скрытая теплота плавления составляет 236,1 кДж/кг.
Применяя в смеси хлористый кальций (29,9%), можно понизить температуру плавления смеси до -55°С, в этом случае
r = 214 кДж/кг.
Сублимация — переход вещества из твердого состояния в газообразное, минуя жидкую фазу, с поглощением теплоты. Для охлаждения и замораживания пищевых продуктов, а также их хранения и транспортировки в замороженном состоянии широко используют сублимацию сухого льда (твердой двуокиси углерода). При атмосферном давлении сухой лед, поглощая теплоту из окружающей среды, переходит из твердого состояния в газообразное при температуре -78,9 °С. Удельная теплота сублимации t = 571 кДж/кг.
Сублимация замороженной воды при атмосферном давлении происходит при сушке белья зимой. Этот процесс лежит в основе промышленной сушки пищевых продуктов (сублимационная сушка). Для интенсификации сублимационной сушки в аппаратах (сублиматорах) поддерживают с помощью вакуумных насосов давление ниже атмосферного.
Испарение — процесс парообразования, происходящий со свободной поверхности жидкости. Его физическая природа объясняется вылетом молекул, обладающих большой скоростью и кинетической энергией теплового движения, из поверхностного слоя. Жидкость при этом охлаждается. В холодильной технике этот эффект используют в градирнях для охлаждения воды и в испарительных конденсаторах для передачи теплоты конденсации к воздуху.
При атмосферном давлении и температуре О °С скрытая теплота . испарения воды г=2509 кДж/кг, при температуре 100°С г= ==2257 кДж/кг.
Кипение — процесс интенсивного парообразования на поверхности нагрева за счет поглощения теплоты. Кипение жидкости при низкой температуре является одним из основных процессов в парокомпрессионных холодильных машинах. Кипящую жидкость называют холодильным агентом (сокращенно — хладагент), а аппарат, где он кипит, забирая теплоту от охлаждаемого вещества,- испарителем (название не совсем точно отражает суть происходящего в аппарате процесса). Количество теплоты Q, .подводимое к кипящей жидкости, определяют по формуле:
Q=Mr
где М — масса жидкости, превратившейся в пар. Кипение однородного («чистого») вещества происходит при постоянной температуре, зависящей от давления. С изменением давления меняется и температура кипения. Зависимость температуры кипения от давления кипения (давления фазового равновесия) изображают кривой, называемой кривой упругости насыщенного пара.
Для наиболее распространенного в холодильной технике хладагента — аммиака — такая кривая приведена на рис. 2. Атмосферному давлению, равному 0,1 МПа, соответствует температура кипения аммиака -33 °С, давлению 1,2 МПа — температура 30 °С.
РИС. 2. Кривая упругости насыщенного пара аммиака. Значения скрытой (удельной) теплоты парообразования и давления кипения для некоторых хладагентов при температуре кипения -15 °С приведены в таблице.
Источник